2018年の神経科学進歩:がん、神経発達、神経変性疾患への新たな治療法?2018年の神経科学研究の最前線:アルツハイマー病、多発性硬化症、脳卒中後疼痛
2018年12月、神経疾患研究に革新!グリオ−マの予後改善、小脳発達抑制の発見、多発性硬化症治療の可能性、脊髄損傷後の運動回復への手がかり、脳卒中後疼痛メカニズム解明… 多様な研究成果が発表され、神経系の理解を深め、新たな治療法開発への道を開きます。ミクログリアの役割にも注目!
💡 2018年発表の論文から、アルツハイマー病、多発性硬化症、脳卒中後疼痛など、様々な疾患に対する理解が深まった。
💡 新たな治療法開発の可能性を示唆する研究が複数発表され、神経科学分野の進歩を示した。
💡 各疾患のメカニズム解明に貢献し、ミクログリアやプロスタサイクリンなど、新たな治療標的が発見された。
本日は、2018年の神経科学分野における重要な進展について、三つの章に分けてご紹介していきます。
各章では、それぞれの研究がもたらす可能性と、今後の展望についてもお話しします。
2018年の神経科学における進展:がん、神経発達、神経変性疾患への新たな光
IDH1変異グリオ−マの予後改善につながる遺伝子は?
G0S2遺伝子のメチル化。
2018年の神経科学分野における進展は、がん、神経発達、神経変性疾患に対する理解を深め、新たな治療法開発の可能性を示しました。
特に、アルツハイマー病とLRRK2に関する研究が進展しました。

✅ 2024年8月20日に発表された論文では、慢性的な神経活動の亢進が、アルツハイマー病モデルマウスにおいてタウの伝播を悪化させることを発見しました。
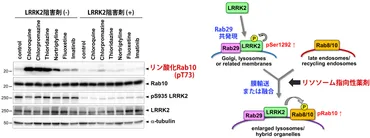
✅ 2024年1月23日に発表された論文では、LRRK2がリソソームストレスに応答して活性化し、α-シヌクレイン線維をエクソソームを介して細胞外に放出するメカニズムを、マクロファージ系細胞において明らかにしました。
✅ 2024年1月17日に発表された論文では、LRRK2がリソソームのストレス応答を促進するために、V-ATPase-ATG16L1軸によってリソソームにリクルートされることを明らかにしました。
さらに読む ⇒東京大学大学院 医学系研究科 神経病理学分野出典/画像元: http://www.neuropathology.m.u-tokyo.ac.jp/news.htmlアルツハイマー病モデルマウスでのタウ伝播の悪化や、LRRK2の新たなメカニズムの解明は、今後の治療戦略を考える上で非常に重要な知見だと思います。
2018年12月には、様々な神経系の疾患に対する理解を深め、新たな治療法開発の可能性を示す複数の研究成果が発表されました。
Fukunaga T.らは、G0S2遺伝子のメチル化がIDH1変異グリオ−マの浸潤を抑制し、予後を改善することを示唆しました。
一方、Abe Y.らは、ペルオキシソーム生合成の欠陥がBDNF-TrkB経路を介した小脳の発達を抑制することを発見しました。
えー、すごいやん!脳ってホンマ複雑やけど、こんなん解明されたら、めっちゃ未来明るいやん!でも、むずくて全然わからんかったー!
多発性硬化症と脊髄損傷へのアプローチ
多発性硬化症と脊髄損傷、RGM-AとNeuropilin-1の役割とは?
RGM-A阻害が進行抑制、Neuropilin-1が運動回復に重要。
多発性硬化症と脊髄損傷に対するアプローチとして、神経再生を促進する物質「プロスタサイクリン」の発見は画期的です。
軸索再生力を高めるメカニズムの解明は、治療薬開発の大きな一歩となるでしょう。
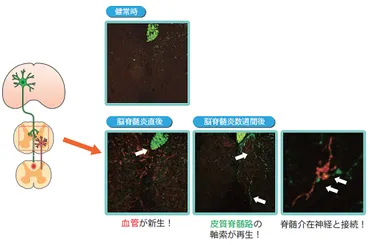
✅ 多発性硬化症の治療法開発のため、神経再生を促進する物質「プロスタサイクリン」を発見。
✅ 血管が放出する「プロスタサイクリン」が軸索の再生力を高めることを解明し、マウスの症状を改善。
✅ 今回の研究成果は、中枢神経損傷に対する新たな分子標的治療薬の開発につながる可能性を示唆。
さらに読む ⇒国立研究開発法人 科学技術振興機構出典/画像元: https://www.jst.go.jp/pr/announce/20121008/index.htmlプロスタサイクリンによる軸索再生促進は、多発性硬化症の治療に希望をもたらしますね。
今後の臨床応用が大いに期待できます。
神経細胞のガイダンス分子RGM-Aを阻害することで、多発性硬化症のマウスモデルにおける二次進行を抑制できることがTanabe S.らによって示されました。
また、Nakanishi T.らは、Neuropilin-1が皮質脊髄路線維の剪定に関与し、脊髄損傷後の運動回復に必要であることを示唆しました。
いやー、すごいっすね!プロスタサイクリンとか、なんかカッコいいっすね!俺もなんか、頑張ろ!
次のページを読む ⇒
脳卒中後疼痛の謎に迫る!ミクログリアが感覚回路を再編成し、疼痛に関与。出血誘発性疼痛への影響も探る、画期的な研究。